ong noi loc
New member
- Xu
- 26

III - TÍNH CHẤT HÓA HỌC
1. Tính axit và ảnh hưởng của nhóm thế
Do mật độ electron ở nhóm OH- dịch chuyển về phía nhóm C=O, nguyên tử H của nhóm OH trở nên linh động nên axit cacboxylic điện li không hoàn toàn trong nước theo cân bằng:
R−COOH + H2O ⇌ H[SUB]3[/SUB]O[SUP]+[/SUP]+ R−COO[SUP]−[/SUP]
Ka=[H3O+].[RCOO−] / [RCOOH]Ka là mức đo lực axit: Ka càng lớn thì axit càng mạnh và ngược lại. Lực axit của axit caboxylic phụ thuộc vào cấu tạo của nhóm nguyên tử liên kết với nhóm cacboxyl (kí hiệu chung là R).
Axit cacboxylic là những axit yếu. Tuy vậy, chúng có đầy đủ tính chất của một axit như : làm đỏ quỳ tím, tác dụng với kim loại giải phóng hiđro, phản ứng với bazơ, đẩy được axit yếu hơn ra khỏi muối.
* Trong các axit no đơn chức, axit fomic (R là H) mạnh hơn cả. Các nhóm ankyl đẩy electron về phía nhóm cacboxyl nên làm giảm lực axit:
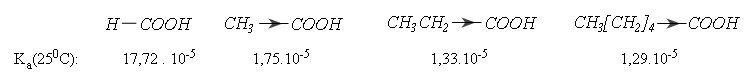
Thí dụ:

a) Phản ứng với ancol (phản ứng este hóa)
* Thực nghiệm: Trong những bình thủy tinh hàn kín chứa hỗn hợp phản ứng, được đun nóng ở 80[SUP]o[/SUP]C. Sau phản ứng, chuẩn độ bằng dung dịch NaOH1M ta xác định được lượng axit axetic, từ đó tính được số mol este, nE, ở mỗi bình. Kết quả thực nghiệm được biểu diễn trên đồ thị ở hình dưới.

* Kết luận: Phản ứng của axit axetic với etanol xúc tác axit là phản ứng thuận nghịch
CH3−CO−OH + C2H5−O−H ⇌ CH3−CO−OC2H5 + H2O
axit axetic............etanol...................etyl axetat..............
Một cách tổng quát, phản ứng giữa axit cacboxylic và ancol được viết như sau:axit axetic............etanol...................etyl axetat..............

Chiều thuận là phản ứng este hóa, chiều nghịch là phản ứng thủy phân este.
b) Phản ứng tách nước liên phân tử
Khi cho tác dụng với P2O5, hai phân tử axit tách đi một phân tử nước tạo thành phân tử anhiđrit axit. Thí dụ:
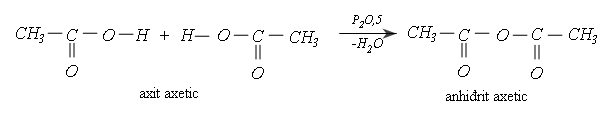
3. Phản ứng ở gốc hiđrocacbon
a) Phản ứng thế ở gốc no
Khi dùng photpho (P) làm xúc tác, Cl chỉ thế cho H ở cacbon bên cạnh nhóm cacboxyl. Thí dụ:
CH3CH2CH2COOH + Cl[SUB]2[/SUB] → CH3CH2−CHCl−COOH + HCl
b) Phản ứng thế ở gốc thơm
Nhóm cacboxyl ở vòng benzen định hường cho phản ứng thế tiếp theo vào vị trí meta và làm cho phản ứng khó khăn hơn so với thế vào benzen:
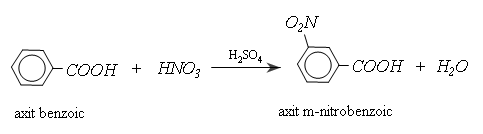
c) Phản ứng cộng vào gốc không no
Axit không no tham gia phản ứng cộng H2,Br2,Cl2... như hiđrocacbon không no.
Thí dụ:
CH3[CH2]7CH=CH[CH2]7COOH + H[SUB]2[/SUB] → CH3[CH2]7CH2CH2[CH2]7COOH
axit oleic.................................................axit stearic
CH3CH=CHCOOH + Br[SUB]2[/SUB] → CH3CHBr−CHBrCOOH
axit oleic.................................................axit stearic
CH3CH=CHCOOH + Br[SUB]2[/SUB] → CH3CHBr−CHBrCOOH
Sửa lần cuối bởi điều hành viên:
