ong noi loc
New member
- Xu
- 26
I. Sơ lược.
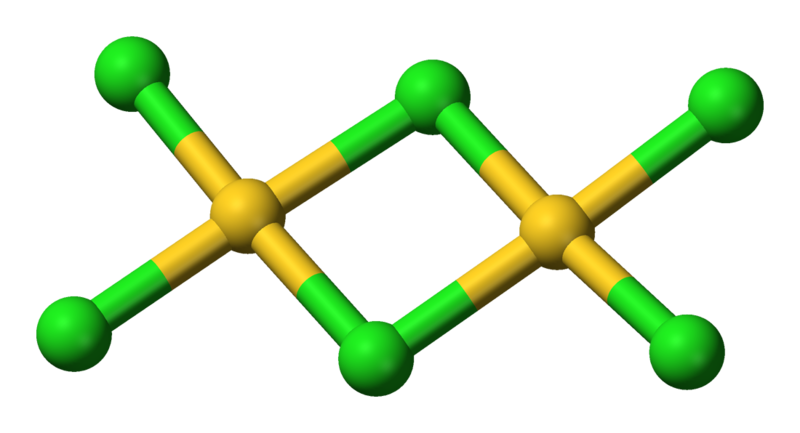
Vàng (III) clorua, theo truyền thống được gọi là clorua vàng, là một hóa chất hợp chất của vàng và clo . Với công thức phân tử của Au[SUB]2[/SUB]Cl[SUB]6[/SUB], trichloride vàng tên là một đơn giản hóa, đề cập đến công thức kinh nghiệm. Các chữ số La Mã trong tên chỉ ra rằng vàng có một trạng thái ôxi hóa +3, mà là phổ biến các hợp chất vàng. Đó cũng là một clorua liên quan đến vàng, vàng (I) clorua (AuCl). chloroauric axit , HAuCl4, sản phẩm được hình thành khi vàng tan trong nước cường toan , đôi khi được gọi là "clorua vàng", "axit vàng trichloride" hoặc thậm chí "vàng (III) clorua trihydrat." Vàng (III) clorua là rất dễ hút ẩm và hòa tan cao trong nước cũng như ethanol . Nó phân hủy ở trên 160 ° C hoặc trong ánh sáng.
II.Điều chế
Vàng clorua (III) thường được chuẩn bị bằng cách đi qua khí clo bột vàng ở mức 180 ° C:
Tiếp xúc với nước, AuCl[SUB]3[/SUB] hình thức một loạt các loài, đôi khi được mô tả như AuCl3.H2O và bazơ liên hợp của nó [AuCl[SUB]3[/SUB](OH)][SUP]-[/SUP].
Phản ứng với các chất khử như hydrogen peroxide hoặc Fe[SUP]2+ [/SUP]làm vàng nguyên tố để được tủa từ dung dịch
Khan AuCl[SUB]3[/SUB] bắt đầu phân hủy để AuCl khoảng 160 ° C, tuy nhiên, điều này lần lượt trải qua disproportionation ở nhiệt độ cao để cung cấp cho kim loại vàng và AuCl[SUB]3[/SUB].
HCl + AuCl3 → H[SUP]+[/SUP] + [AuCl[SUB]4[/SUB]] [SUP]-[/SUP]
Nguồn chloride khác, chẳng hạn như KCl , cũng chuyển đổi AuCl3 vào AuCl[SUB]4[/SUB][SUP]-[/SUP] . Dung dịch nước của AuCl[SUB]3[/SUB] phản ứng với cơ sở dịch nước như natri hydroxit để tạo thành một kết tủa của Au(OH)[SUB]3[/SUB], sẽ hòa tan trong NaOH dư thừa để tạo thành aurate natri (NaAuO[SUB]2[/SUB]). Nếu đun nóng nhẹ nhàng, Au(OH)[SUB]3[/SUB] phân hủy (III) oxit vàng , Au[SUB]2[/SUB]O[SUB]3[/SUB], và sau đó vàng kim loại.
Vàng (III) clorua là điểm khởi đầu cho sự tổng hợp của các hợp chất vàng khác. Ví dụ, phản ứng với potassium cyanide sản xuất tan trong nước phức tạp , K[Au(CN)[SUB]4[/SUB]]:
AuCl[SUB]3[/SUB] + 4KCN → K[Au(CN)[SUB]4[/SUB]] + 3KCl
Vàng (III) clorua, theo truyền thống được gọi là clorua vàng, là một hóa chất hợp chất của vàng và clo . Với công thức phân tử của Au[SUB]2[/SUB]Cl[SUB]6[/SUB], trichloride vàng tên là một đơn giản hóa, đề cập đến công thức kinh nghiệm. Các chữ số La Mã trong tên chỉ ra rằng vàng có một trạng thái ôxi hóa +3, mà là phổ biến các hợp chất vàng. Đó cũng là một clorua liên quan đến vàng, vàng (I) clorua (AuCl). chloroauric axit , HAuCl4, sản phẩm được hình thành khi vàng tan trong nước cường toan , đôi khi được gọi là "clorua vàng", "axit vàng trichloride" hoặc thậm chí "vàng (III) clorua trihydrat." Vàng (III) clorua là rất dễ hút ẩm và hòa tan cao trong nước cũng như ethanol . Nó phân hủy ở trên 160 ° C hoặc trong ánh sáng.

Vàng clorua (III) thường được chuẩn bị bằng cách đi qua khí clo bột vàng ở mức 180 ° C:
2 Au + 3 Cl[SUB]2 [/SUB]→ 2 AuCl[SUB]3[/SUB]
Một phương pháp chuẩn bị, là phản ứng Ngoài ra, vàng (3+) phản ứng với clo để sản xuất tetrachloridoaurate , sau đó, tetrachloridoaurate hydro được làm nóng để loại bỏ khí chlorane. Vàng (3+) được sản xuất bằng cách oxy hóa với axit nitric hiện diện trong nước cường toan :Au + HNO[SUB]3[/SUB] + 3HCl ------------> AuCl[SUB]3[/SUB] + NO + 2H2O

III. Tính chất
Tiếp xúc với nước, AuCl[SUB]3[/SUB] hình thức một loạt các loài, đôi khi được mô tả như AuCl3.H2O và bazơ liên hợp của nó [AuCl[SUB]3[/SUB](OH)][SUP]-[/SUP].
Phản ứng với các chất khử như hydrogen peroxide hoặc Fe[SUP]2+ [/SUP]làm vàng nguyên tố để được tủa từ dung dịch
Khan AuCl[SUB]3[/SUB] bắt đầu phân hủy để AuCl khoảng 160 ° C, tuy nhiên, điều này lần lượt trải qua disproportionation ở nhiệt độ cao để cung cấp cho kim loại vàng và AuCl[SUB]3[/SUB].
AuCl[SUB]3 [/SUB]→ AuCl + Cl[SUB]2[/SUB] (> 160 ° C)
3 AuCl → AuCl[SUB]3[/SUB] + 2Au (> 420 ° C)
AuCl[SUB]3[/SUB] là Lewis có tính axit và dễ dàng tạo phức . Ví dụ, nó phản ứng với axit clohydric để hình thành axit chloroauric (HAuCl[SUB]4[/SUB]):3 AuCl → AuCl[SUB]3[/SUB] + 2Au (> 420 ° C)
HCl + AuCl3 → H[SUP]+[/SUP] + [AuCl[SUB]4[/SUB]] [SUP]-[/SUP]
Nguồn chloride khác, chẳng hạn như KCl , cũng chuyển đổi AuCl3 vào AuCl[SUB]4[/SUB][SUP]-[/SUP] . Dung dịch nước của AuCl[SUB]3[/SUB] phản ứng với cơ sở dịch nước như natri hydroxit để tạo thành một kết tủa của Au(OH)[SUB]3[/SUB], sẽ hòa tan trong NaOH dư thừa để tạo thành aurate natri (NaAuO[SUB]2[/SUB]). Nếu đun nóng nhẹ nhàng, Au(OH)[SUB]3[/SUB] phân hủy (III) oxit vàng , Au[SUB]2[/SUB]O[SUB]3[/SUB], và sau đó vàng kim loại.
Vàng (III) clorua là điểm khởi đầu cho sự tổng hợp của các hợp chất vàng khác. Ví dụ, phản ứng với potassium cyanide sản xuất tan trong nước phức tạp , K[Au(CN)[SUB]4[/SUB]]:
AuCl[SUB]3[/SUB] + 4KCN → K[Au(CN)[SUB]4[/SUB]] + 3KCl
