nguoiconhieuhoc
New member
- Xu
- 0
cho hỏi tại sao trong nhóm IA đi từ Li đến Cs (trừ Na) khối lượng riêng của các kim loại tăng dần?
cho hỏi tại sao trong nhóm IA đi từ Li đến Cs (trừ Na) khối lượng riêng của các kim loại tăng dần?
Công thức tính khối lượng riêng của kim loại:
\[D = \frac{3.M.P}{4.\pi.r^3.N_A}\]
Trong đó:
M: nguyên tử lượng.
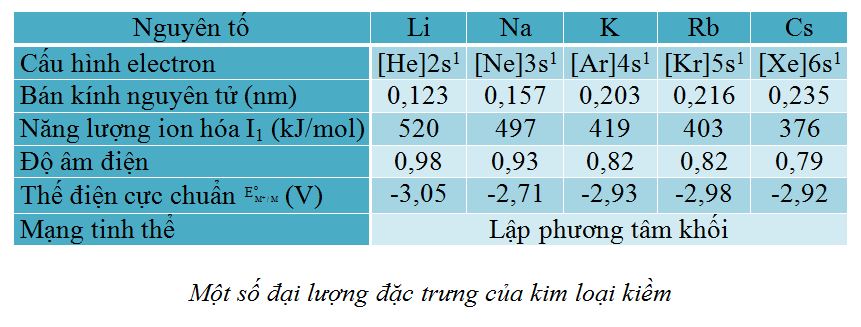
P: độ đặc khít của mạng tinh thể, ở đây các kim loại nhóm IA có kiểu mạng tinh thể lập phương tâm khối nên P = 68%.
r: bán kính nguyên tử.
Xét cơ bản từ Liti đến Cs, ta thấy tỷ số M/r^3 tăng dần, do đó khối lượng riêng tăng dần. Riêng trường hợp của Natri tăng đột biến (khi xét từ Liti đến Kali), có thể giải thích như sau: ở chu kỳ 1 và 2 thì bán kính nguyên tử tăng không đáng kể so với độ tăng của nguyên tử lượng, nhưng bắt đầu từ chu kỳ 3 trở đi thì bán kính nguyên tử tăng rất nhanh nên tỷ lệ M/r^3 có sự chênh lệch giữa Na với K. Điều này giải thích vì sao D[SUB]Na[/SUB] lớn hơn D[SUB]K[/SUB]
